Aprovado no Senado, projeto avança brasileira na vanguarda científica, contudo, questiona proteção a voluntários. Mão de obra qualificada, genética populacional, burocracia, país participação, regulamento, parágrafos críticos, econômico, ambiental, inovação, testes, direitos voluntários. (142 caractères)
Desde que o médico escocês James Lind descobriu, no século XVIII, como salvar marinheiros que pereciam por escorbuto, doença causada pelo déficit de vitamina C, adicionando frutas cítricas à dieta, as pesquisas clínicas se tornaram a melhor maneira de comprovar quais medidas realmente fazem a diferença na saúde e de desenvolver novos fármacos por meio da mobilização de mão de obra qualificada acompanhados com rigor.
Hoje em dia, os estudos clínicos são fundamentais para avanços médicos e científicos, permitindo que a eficácia de tratamentos seja comprovada de forma segura e confiável. Participar de pesquisas clínicas pode representar uma oportunidade de contribuir para o progresso da medicina e ter acesso a terapias inovadoras, sendo essencial para o desenvolvimento de novas soluções de saúde.
Projeto de Lei Para Modernizar Regras em Pesquisas Clínicas
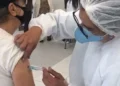
Das vacinas aos analgésicos, dos tratamentos celulares aos medicamentos em geral, a validade de qualquer produto farmacêutico requer a realização de pesquisas clínicas com seres humanos. Esses estudos são essenciais para comprovar a segurança e eficácia dos tratamentos, indo além dos testes em células e animais.
O Brasil desponta como uma peça-chave nesse cenário, graças à sua mão de obra qualificada e à diversidade genética da população. No entanto, deparando-se com obstáculos estruturais e burocráticos, o país enfrenta limitações na participação ativa no campo da pesquisa científica.
Foi nesse contexto que o Senado aprovou um projeto de lei (PL) em caráter de urgência, visando atualizar as normas que regem as pesquisas clínicas no país. O intuito é impulsionar o Brasil como um participante relevante no cenário global de estudos científicos, promovendo assim mudanças significativas para o setor.
A discussão sobre as mudanças no marco regulatório dos ensaios clínicos teve seu início em 2015 e tem evoluído desde então. O projeto buscou flexibilizar as regras estabelecidas em 1996, permitindo uma participação mais ágil do Brasil em pesquisas internacionais.
Parágrafos cruciais do PL foram alvo de intensos debates a partir de 2017, resultando em um novo documento que agora aguarda sanção presidencial. Esse texto atualizado foi recebido com uma mistura de aplausos e críticas.
Representantes da indústria farmacêutica e parlamentares elogiam as mudanças propostas, destacando a redução da burocracia e a facilitação da inclusão do país em estudos multicêntricos. Renato Porto, presidente da Interfarma, acredita que tais alterações podem elevar a posição do Brasil no ranking de pesquisas clínicas no mundo.
A diversidade genética da população brasileira surge como um grande atrativo para estudos globais, sendo um diferencial importante para o avanço da ciência. No entanto, garantir a lisura dos testes e proteger os direitos dos voluntários são pontos indiscutíveis.
O projeto de lei reconhece a importância dessas questões éticas e estabelece medidas para assegurar a transparência e a proteção dos participantes dos ensaios clínicos. A necessidade de avaliação pelos órgãos competentes e a obrigatoriedade dos patrocinadores arcarem com os custos dos estudos foram mantidas, evidenciando o compromisso com a ética e a segurança dos participantes.
O acesso aos tratamentos testados será garantido aos voluntários por até cinco anos após sua disponibilização comercial, ressaltando a preocupação com a saúde e o bem-estar da população. Essas medidas trazem impactos positivos não apenas para a economia, mas também para o avanço da ciência e a proteção dos direitos humanos na área das pesquisas clínicas.
Fonte: @ Veja Abril







Comentários sobre este artigo